Когда в апреле 2016 года доктор Джон Джанг из Центра репродукции «Новая Надежда» в Нью-Йорке (США) впервые заявил о том, что благодаря их усилиям в мире родился первый ребенок, зачатый с помощью технологии ЭКО от трех родителей, ученые забили тревогу. Одни были обеспокоены этической стороной данного вопроса, другие — медицинской. Однако, спустя месяцы жарких дебатов, в апреле 2017 года команда доктора Д. Джанга опубликовала статью в журнале Reproductive Biomedicine Online, где более подробно рассказала об этом клиническом случае [1]. Однако, как минимум один вопрос все равно оставался актуальным: повлияет ли этот метод зачатия на здоровье ребенка в отдаленном будущем?
Доктор J. Zhang держит первого в мире новорожденного мальчика, который был зачат посредством технологии ЭКО от трех родителей
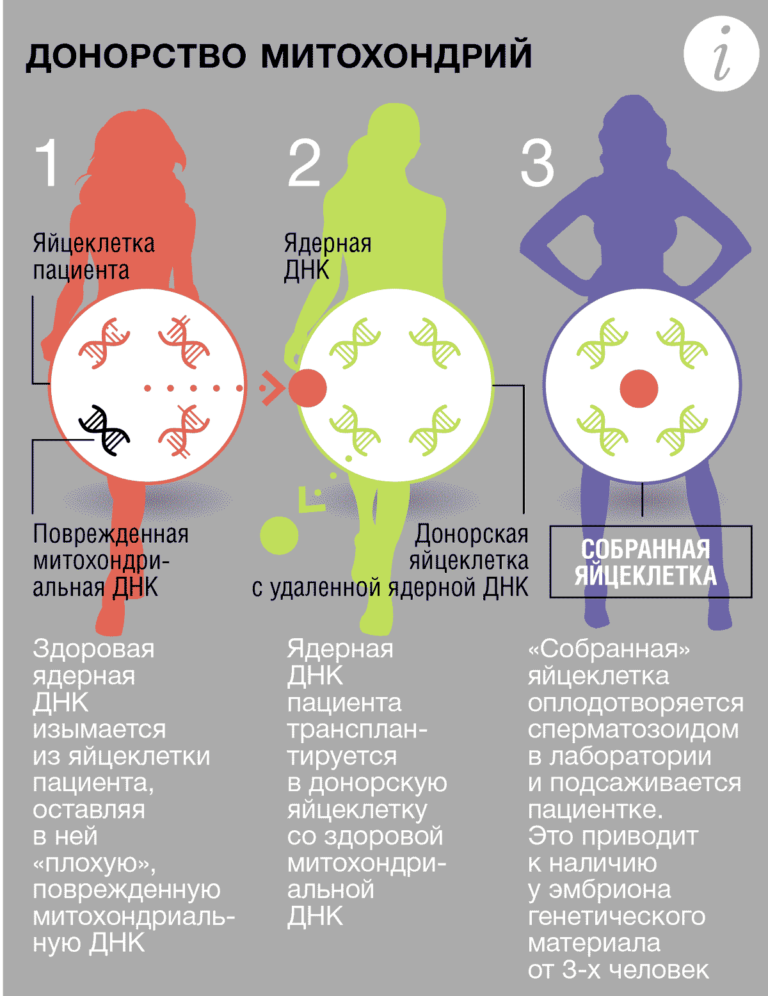
Итак, что же из себя представляет техника ЭКО от трех родителей? Данная манипуляция позволяет «совместить» генетический материал трех человек — ДНК отца, ДНК матери и митохондриальную ДНК (мтДНК) донора яйцеклетки — с тем, чтобы получить здоровый эмбрион. Мутации в мтДНК обычно приводят к тяжелым митохондриальным заболеваниям таким как мышечная дистрофия, амиотрофический латеральный склероз и др. Поскольку мтДНК наследуется ребенком только из яйцеклетки, располагаясь при этом в цитоплазме клетки, то есть вне ядра, то дети женщины — носителя митохондриального заболевания имеют очень высокий риск развития данных патологий. Таким образом, процедура ЭКО от трех родителей представляет собой метод ВРТ, при котором дефектная митохондрия матери заменяется на здоровую донорскую, при этом генетический материал, содержащийся в ядре яйцеклетки, остается нетронутым. Кроме того, если при этом проводить отбор эмбрионов по полу, выбирая только здоровые эмбрионы мужского пола, то можно полностью предотвратить передачу митохондриальных заболеваний последующим поколениям в семье [2]. В случае, о котором рапортовали американские врачи-ученые, команда доктора Д. Джанга удалила из здоровой донорской яйцеклетки ядро, заменив его ядром из яйцеклетки пациентки, которая являлась носителем редкого неврологического заболевания — синдрома Лея — оставив таким образом нетронутой мтДНК донора [1]. Синдром Лея является наследственным заболеванием центральной нервной системы из группы митохондриальных энцефаломиелопатий, обусловленным нарушением обмена тиамина и проявляющееся в раннем детском возрасте симптомами поражения серого вещества головного и спинного мозга. После манипуляций с яйцеклетками эмбриологи оплодотворили полученную яйцеклетку спермой мужа и, получив эмбрион, подсадили его в матку пациентки. В апреле 2016 года пациентка родила мальчика. Однако, авторы упоминают о том, что в процессе проведения данной процедуры малая часть «больной» ДНК все равно была перенесена в донорскую яйцеклетку, что было, по сути, неизбежным. Будет ли это иметь отдаленные последствия для здоровья ребенка в будущем — открытый вопрос. Некоторые ученые предполагают, что даже следы материнской «больной» мтДНК могут стать причиной неправильной работы здоровой донорской мтДНК. Процент поврежденных митохондрий может варьироваться в зависимости от ткани. Zhang et al. (2017) пишут о том, что в моче рожденного мальчика обнаруживается только 2% клеток с материнской мтДНК, однако в иссеченной крайней плоти их уже 9%. Науке неизвестно, какое количество «больных» митохондрий может привести к развитию клинически значимых симптомов митохондриального заболевания у ребенка, который является носителем генетического материала от двух женщин. Однако, в исследовании на мышах было показано, что такая «смесь» митохондрий может привести к манифестации неврологических заболеваний или метаболических нарушений [3]. К сожалению, данный клинический случай не позволит проследить отдаленные последствия этой процедуры в отношении здоровья мальчика: родители ребенка отказались от проведения последующих анализов и тестирования функций митохондрий их сына при отсутствии на то медицинский показаний. Многие ученые высказывают оправданные опасения, что, возможно, они слишком сильно спешат заявить об этой технике как об эффективном методе лечения для своих пациентов в то время, пока они еще очень мало знают о том, каковы будут отдаленные исходы ЭКО от трех родителей. «Мы не знаем, безопасна ли эта техника,» — говорит ученый-биоэтик из университета Висконсин-Мэдисон Alta Charao. При этом доктор Джанг заявляет, что они обязательно продолжат тестирование данной методики с использованием яйцеклеток пациенток в возрасте от 42 до 47 лет. Его команда планирует исследовать, может ли митохондрия из здоровой яйцеклетки более молодого донора стимулировать способность к оплодотворению и нормальному развитию яйцеклетки более зрелой женщины.
Однако, в последние два года не только в США стали активно осваивать эту технологию. В начале февраля 2015 года подавляющее большинство Палаты общин Великобритании проголосовало за разрешение ученым проводить дальнейшие исследования по технике замены митохондриальной ДНК. Таким образом, Великобритания стала первой страной в мире, в которой был легализован данный метод для использования в клинической практике [2].
Согласно последнему исследованию, которое было опубликовано в авторитетном журнале New England Journal of Medicine, около 2500 женщин Великобритании нуждаются в митохондриальном донорстве. Английские ученые подсчитали, что ЭКО от трех родителей позволит каждый год предотвращать более 150 случаев тяжелых редких заболеваний у детей в их стране.
Как известно, в России данный метод пока не нашел свое применение. Поэтому врачам-репродуктологам приходится усиленно искать другие методы «улучшения» материнских яйцеклеток с целью увеличения шансов на успешное ЭКО и рождение здорового ребенка. В 2017 году в журнале Gynecologic and Obstetric Investigation были опубликованы результаты весьма интересного клинического исследования, проведенного на базе Венского медицинского университета в Австрии [4]. Исследователи заявили о том, что они нашли препарат, который может достоверно улучшать качество яйцеклеток и, соответственно, качество полученных эмбрионов в циклах ЭКО. В общей сложности в исследование было включено 100 женщин, которым проводили ЭКО или ИКСИ в Венском медицинском университете в период с 2013 по 2015 год. Участниц рандомизировали на две равные группы: до стимуляции яичников представительницам первой группы назначили комплекс микронутриентов ─ фолиевую кислоту (800 мкг), антиоксиданты селен (70 мкг), витамин Е (30 мг) и катехины (4 мг); а также глицирризин (12 мг), диосгенин (32 мг), экстракт дамианы (90 мг) и омега-3 жирные кислоты (500 мг); все эти компоненты пациенткам выписали в составе препарата «ПРОфертил фимейл». Женщинам из второй (контрольной) группы прописали только фолиевую кислоту в суточной дозе 400 мкг. Препараты рекомендовали принимать не менее 28 дней, но не более 56 дней до стимуляции яичников. Для последней пациенткам вводили 10 тыс. МЕ ХГЧ, а спустя 35 ч проводили процедуру забора яйцеклеток. Для оплодотворения использовали стандартные методики ЭКО/ИКСИ. Перенос эмбрионов проводили на 3 или 5 дни после забора яйцеклеток. Для поддержания лютеиновой фазы всем пациенткам назначался прогестерон (интравагинально) в суточной дозе 600 мг.
 Обе группы женщин по количеству забранных и оплодотворённых яйцеклеток статистически значимо не различались. Однако, в группе пациенток, принимавших комплекс ПРОфертил фимейл, эмбрионов высокого качества было получено в 1,6 раза больше, чем среди тех, кто принимал только фолиевую кислоту ─ 58 против 36% (ОР 1,6; 95% ДИ 1–2,6). Кроме того, было установлено, что частота наступления беременности у пациенток из первой группы также была выше, чем у участниц из второй группы ─ 40% против 26% (ОР 1,5; 95% ДИ 0,8–2,9), хотя различия и оказались статистически не значимыми.
Обе группы женщин по количеству забранных и оплодотворённых яйцеклеток статистически значимо не различались. Однако, в группе пациенток, принимавших комплекс ПРОфертил фимейл, эмбрионов высокого качества было получено в 1,6 раза больше, чем среди тех, кто принимал только фолиевую кислоту ─ 58 против 36% (ОР 1,6; 95% ДИ 1–2,6). Кроме того, было установлено, что частота наступления беременности у пациенток из первой группы также была выше, чем у участниц из второй группы ─ 40% против 26% (ОР 1,5; 95% ДИ 0,8–2,9), хотя различия и оказались статистически не значимыми.
Список использованной литературы
- Zhang J. et al. Live birth derived from oocyte spindle transfer to prevent mitochondrial disease // Reprod. Biomed. Online. 2017. Vol. 34, № 4. P. 361–368.
- Zhang X., Wang S. From the first human gene-editing to the birth of three-parent baby // Sci. China Life Sci. 2016. Vol. 59, № 12. P. 1341–1342.
- Wallace D.C., Chalkia D. Mitochondrial DNA genetics and the heteroplasmy conundrum in evolution and disease // Cold Spring Harb Perspect Biol. 2013. Vol. 5:a021220.
- Nouri K. et al. The Impact of a Standardized Oral Multinutrient Supplementation on Embryo Quality in in vitro Fertilization/Intracytoplasmic Sperm Injection: A Prospective Randomized Trial // Gynecol Obstet Invest. 2017. Vol. 82. P. 8–14.